導入:高校入試化学は「用語+計算」が得点源になる
高校入試理科の中でも、化学分野は「覚えれば取れる問題」と「理解して計算できないと取れない問題」がはっきり分かれる分野です。
特に入試本番では、用語問題で確実に点を取り、計算問題で差をつけることが合格への近道になります。
化学は暗記だけでなく計算問題で差がつく
中学校の化学では、
- 化学変化の名称・用語
- 化学反応式
- 質量保存の法則
- イオン・電池・電気分解
- 質量・体積・濃度の計算
といった内容が出題されます。
一見すると暗記中心に見えますが、実際の高校入試では「用語を知っている前提」で計算や理由説明をさせる問題が非常に多くなっています。
実際、文部科学省の学習指導要領(中学理科 – 化学分野)では、実験手順において計算して結果を出し、結果に関する考察も行うと定められています。
見通しをもって解決する方法を立案して,実験を行い,得られた結果をグラフ化することを通して分析して解釈し規則性を見いだして,表現させるようにする
文部科学省『中学校学習指導要領解説(理科 – 化学分野の目標)』より引用
そのため、
- 用語をあいまいに覚えている
- 計算問題を後回しにしている
という状態では、平均点は取れても上位校合格ラインには届きません。
一問一答を軸に、入試対応力を高める記事です
本記事は、
「高校入試 化学 一問一答」の決定版として、
- 入試頻出用語を一問一答で即チェック
- 計算問題につながる考え方を簡潔に整理
- 暗記 → 理解 → 得点化までを一気に進められる
構成になっています。
単なる丸暗記用の一問一答ではなく、
「なぜそうなるのか」「入試ではどう問われるのか」まで意識した内容にすることで、実戦力を高めることを目的としています。
メイン記事「高校入試 理科 一問一答」との使い分け
この記事は、
▶ 化学分野に特化した一問一答・対策記事です。
理科全体を横断的に復習したい場合は、
メイン記事である
▶ 「高校入試 理科 一問一答|全分野まとめ」
を先に確認するのがおすすめです。
- 親記事:理科全体の一問一答で弱点発見
- 本記事:化学分野を重点的に得点源にする
という使い分けをすることで、最短ルートで入試対策が進みます。
高校入試 化学の出題傾向と勉強法
高校入試の化学分野は、出題パターンがある程度決まっており、正しい勉強法を取れば短期間でも得点が伸びやすいのが特徴です。
ここでは、入試で「何がどう問われるのか」と「どう対策すればよいのか」をセットで解説します。
化学は「用語暗記+計算理解」のセットが必須
高校入試化学で最も重要なのは、
用語暗記と計算理解を切り離さないことです。
入試でよくある出題パターン
実際の入試では、次のような出題が頻出です。
- 用語を答えさせたあと、その内容を使って計算させる
- 化学反応式を書かせたうえで、質量や体積を求めさせる
- イオン名を答えたあと、電池や電気分解の流れを考えさせる
例えば、令和7年度の東京都立高校入試問題で、炭酸水素ナトリウムと酸化銀の熱分解の実験で、水上置換法で複数の試験管に気体を集めた際に、1本目の試験管に集まった気体を実験に使わない理由を記述させる問題が出されており、その後の問題で炭酸水素ナトリウムの質量を求める計算問題が出ています。
(問1)気体を集めた3本の試験管のうち,気体を集め始めて1 本目の試験管に集めた気体を使わなかった理由を,「試験管A」という語句を用いて簡単に書け。
令和7年度 東京都立高校入試問題 理科より引用
(問2)溶け残った加熱前の炭酸水素ナトリウムの質量として適切なのはどれか。
つまり、
☆ 「用語が分からない=計算以前で詰む」
☆ 「計算ができない=暗記だけでは点にならない」
という構造になっています。
NGな勉強例
- 用語集だけを丸暗記して満足
- 計算問題は難しそうだから後回し
- 理解せずに公式だけ覚える
この状態では、一問一答では正解できても、入試本番の応用問題で減点します。
正しい考え方
- 用語は「意味・使われ方」まで理解する
- 計算は「なぜその式になるか」を言葉で説明できるようにする
この2つを同時に進めることが、化学攻略の基本です。
一問一答を計算・記述につなげる勉強法
一問一答は、使い方を間違えると「覚えただけ」で終わる危険な教材ですが、
正しく使えば、計算・記述までつながる最強の基礎トレーニングになります。
実際、東京都など高校入試の問題作成方針においても用語を知っているかどうかだけでなく、説明できるか(表現力)、活用できるかも問うと定めているところが多いです。
基礎的・基本的な知識及び技能をみるとともに,科学的に探究する活動を通して思考力,判断力,表現力等をみる。
東京都教育委員会 学力検査問題等 理科・基本方針より引用
ステップ① 一問一答で「即答レベル」まで仕上げる
まずは、
- 化学変化の名称
- 物質名・イオン名
- 法則・決まり
を見た瞬間に答えられるレベルまで一問一答で固めます。
ここはスピード重視でOKです。
ステップ② 「その用語が出る問題」を必ず想像する
次に重要なのが、
「この用語、入試ではどう問われる?」
と考えることです。
例:
- 「質量保存の法則」
→ 反応前後の質量計算 - 「陽イオン・陰イオン」
→ 電池・電気分解の極の問題
一問一答=問題の入口だと意識するだけで、理解の深さが変わります。
ステップ③ 一文説明できるかをチェック
さらに効果的なのが、
答えを一文で説明する練習です。
例:
- Q. 質量保存の法則とは?
- A. 化学変化の前後で、反応に関わった物質の全体の質量は変わらないという法則。
この練習をすると、
✔ 記述問題
✔ 計算の途中説明
にも強くなります。
短期間で点が伸びやすい単元
化学分野の中でも、入試に直結しやすく、対策効果が高い単元があります。
① 化学変化と化学反応式
- 出題率が非常に高い
- 用語・反応式・計算がセットで問われる
→ 最優先で完成させるべき単元
② 質量保存・質量計算
- 計算問題の定番
- 公式暗記ではなく「考え方」で差がつく
→ 解き方の型を覚えると一気に安定します。
③ イオン・電池・電気分解
- 難しそうに見えるが、パターン問題が多い
- 図と流れを理解すると得点源になる
→ 苦手な人ほど、対策すれば点が伸びやすい分野です。
④ 水溶液の性質(酸・アルカリ)
- 用語暗記+簡単な計算が中心
- 実験問題としても頻出
→ 一問一答との相性が非常に良い単元。
【化学分野】高校入試 一問一答 分野別解説
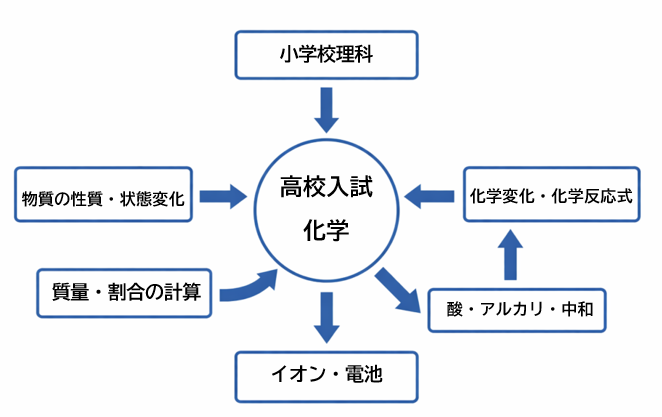
各分野ごとに、①入試に直結する要点解説 → ②一問一答10問(完全暗記用)の構成でまとめています。
一問一答はすべて計算・記述問題につながる基礎知識のみを厳選しています。
物質の性質と状態変化
この分野は「簡単そう」に見えて、実験問題+理由説明で差がつきます。
特に重要なのは、状態が変わっても質量は変わらないという視点です。
固体・液体・気体
- 固体:形・体積が一定
- 液体:体積は一定、形は変わる
- 気体:形・体積ともに変わる
状態変化と質量保存
- 融解・凝固・蒸発・凝縮などの状態変化では、物質そのものは変化しない
- ふた付き容器で考えると、状態変化前後の質量は等しい
一問一答(10問)
- 形も体積も一定な状態は?
→ 固体 - 体積は一定だが形が変わる状態は?
→ 液体 - 形も体積も変わる状態は?
→ 気体 - 固体が液体になる変化を何という?
→ 融解 - 液体が気体になる変化を何という?
→ 蒸発 - 気体が液体になる変化を何という?
→ 凝縮 - 液体が固体になる変化を何という?
→ 凝固 - 状態変化で物質の種類は変わる?
→ 変わらない - 状態変化の前後で成り立つ法則は?
→ 質量保存の法則 - 状態変化は物理変化か化学変化か?
→ 物理変化
化学変化と化学反応式
高校入試化学の最重要分野です。
用語・反応式・質量計算が必ずセットで出題されます。
化学変化/化学反応
- 化学変化:別の物質ができる変化
- 化学反応:化学変化が起こるしくみ
反応前後の物質
- 反応前:反応物
- 反応後:生成物
化学反応式の基本
- 反応物 → 生成物
- 原子の数は左右で必ず等しい
一問一答(10問)
- 別の物質ができる変化を何という?
→ 化学変化 - 化学変化が起こるしくみを何という?
→ 化学反応 - 反応の前にある物質を何という?
→ 反応物 - 反応の後にできる物質を何という?
→ 生成物 - 化学変化で成り立つ重要な法則は?
→ 質量保存の法則 - 化学反応を式で表したものを何という?
→ 化学反応式 - 化学反応式で左側に書くのは?
→ 反応物 - 化学反応式で右側に書くのは?
→ 生成物 - 化学反応式で必ずそろえるものは?
→ 原子の数 - 化学変化は物質の種類が変わる?
→ 変わる
酸・アルカリ・中和
実験問題・記述問題で頻出の分野です。
指示薬の色+中和の生成物は確実に暗記しましょう。
酸性・アルカリ性
- 酸性:水素イオンを出す
- アルカリ性:水酸化物イオンを出す
BTB溶液・リトマス紙
- BTB:酸性=黄色/中性=緑/アルカリ性=青
- リトマス紙:酸性=青→赤/アルカリ性=赤→青
中和反応と生成物
- 酸+アルカリ → 水+塩
一問一答(10問)
- 酸性の水溶液が出すイオンは?
→ 水素イオン - アルカリ性の水溶液が出すイオンは?
→ 水酸化物イオン - BTB溶液で酸性は何色?
→ 黄色 - BTB溶液で中性は何色?
→ 緑色 - BTB溶液でアルカリ性は何色?
→ 青色 - 青色リトマス紙が赤に変わる性質は?
→ 酸性 - 赤色リトマス紙が青に変わる性質は?
→ アルカリ性 - 酸とアルカリが反応することを何という?
→ 中和 - 中和で必ずできる物質は?
→ 水 - 中和で水以外にできる物質は?
→ 塩
イオンと電池
難しそうに見えますが、パターン暗記で得点源になる分野です。
イオン/電解質
- イオン:電気を帯びた粒子
- 電解質:水に溶けると電流が流れる物質
電池のしくみ
- 化学変化によって電流が流れる
- 電子の移動がポイント
陽イオン・陰イオン
- 陽イオン:+
- 陰イオン:−
一問一答(10問)
- 電気を帯びた粒子を何という?
→ イオン - 正の電気を帯びたイオンは?
→ 陽イオン - 負の電気を帯びたイオンは?
→ 陰イオン - 水に溶けて電流が流れる物質は?
→ 電解質 - 電池で電流が流れる原因は?
→ 化学変化 - 電池で移動する粒子は?
→ 電子 - 電子を失ってできるイオンは?
→ 陽イオン - 電子を受け取ってできるイオンは?
→ 陰イオン - 電池は何エネルギーを電気に変える?
→ 化学エネルギー - イオンが存在すると電流は流れる?
→ 流れる
質量・割合の計算問題
計算問題で差がつく最重要分野です。
考え方の型を覚えれば、確実に得点できます。
質量保存の法則
- 化学変化の前後で、反応に関わった物質の全体の質量は等しい
割合計算
- 割合 = 部分 ÷ 全体 × 100
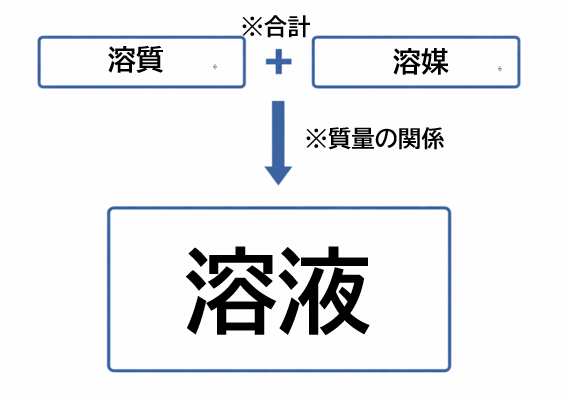
溶質・溶媒・溶液
- 溶質:溶ける物質
- 溶媒:溶かす物質
- 溶液:溶けたあとの全体
一問一答(10問)
- 化学変化前後で成り立つ法則は?
→ 質量保存の法則 - 溶ける物質を何という?
→ 溶質 - 溶かす物質を何という?
→ 溶媒 - 溶質と溶媒を合わせたものは?
→ 溶液 - 溶液の質量は何と何の和?
→ 溶質と溶媒 - 割合を求める基本式は?
→ 部分 ÷ 全体 - 百分率にするには何をかける?
→ 100 - 質量%濃度は何を表す?
→ 溶液中の溶質の割合 - 水に食塩を溶かすと質量は増える?
→ 増える - ふた付き容器で反応すると質量は?
→ 変わらない
計算問題(10問)
【問題1】
400gの食塩水があります。この中に食塩が20g溶けています。
この食塩水の質量パーセント濃度を求めなさい。
【解答】
5%
【解説】
質量%濃度 = 溶質 ÷ 溶液 × 100
= 20 ÷ 400 × 100 = 5%
【問題2】
質量パーセント濃度が10%の食塩水が300gあります。
この中に含まれる食塩の質量は何gですか。
【解答】
30g
【解説】
溶質の質量 = 溶液 × 濃度
= 300 × 0.10 = 30g
【問題3】
水180gに食塩を20g溶かしました。
できた食塩水の質量パーセント濃度を求めなさい。
【解答】
10%
【解説】
溶液の質量 = 180 + 20 = 200g
質量%濃度 = 20 ÷ 200 × 100 = 10%
【問題4】
質量パーセント濃度が5%の食塩水を作りたい。
水380gに加える食塩は何g必要ですか。
【解答】
20g
【解説】
溶液の質量を x とすると
溶質=0.05x
水380g+溶質=溶液
380+0.05x=x
x=400
溶質=0.05×400=20g
【問題5】
120gの水に食塩を加えて、質量パーセント濃度が8%の食塩水を作った。
加えた食塩の質量は何gか。
【解答】
約10.4g
【解説】
溶質を x g とすると
x ÷ (120+x) ×100=8
x=0.08(120+x)
x=9.6+0.08x
0.92x=9.6
x≒10.4g
【問題6】
500gの食塩水があります。
この食塩水に含まれる食塩が25gのとき、質量パーセント濃度を求めなさい。
【解答】
5%
【解説】
25 ÷ 500 ×100 = 5%
→ 数字が変わっても計算の型は同じ。
【問題7】
質量パーセント濃度12%の食塩水250gがあります。
この中に含まれる水の質量は何gですか。
【解答】
220g
【解説】
溶質=250×0.12=30g
水=250−30=220g
【問題8】
200gの水に食塩を溶かして質量パーセント濃度が5%になった。
この食塩水の全体の質量は何gか。
【解答】
約211g
【解説】
溶質を x g とすると
x ÷ (200+x) ×100=5
x=0.05(200+x)
x=10+0.05x
0.95x=10
x≒10.5
溶液=200+10.5≒211g
【問題9】
質量パーセント濃度4%の食塩水が500gあります。
この食塩水に含まれる食塩の質量を求めなさい。
【解答】
20g
【解説】
500×0.04=20g
【問題10】
ある食塩水には食塩が15g溶けています。
この食塩水の質量パーセント濃度が3%のとき、食塩水全体の質量は何gですか。
【解答】
500g
【解説】
溶液=溶質 ÷ 濃度
=15 ÷ 0.03 = 500g
まとめ|入試計算は「型」で解く
高校入試の化学計算は、
- 質量%濃度
- 溶質・溶媒・溶液
- 質量保存の考え方
を型で処理できるかが勝負です。
※なお、理科の計算問題については、以下の記事でさらに詳しく解説し、計算問題も練習用に多数しています。
中学理科の計算問題と分かりやすい解説:酸化銅、密度、濃度、地震、質量、圧力、物体の運動、仕事など
一問一答 → 記述・計算問題への変換(化学編)

高校入試化学で多くの受験生がつまずく原因は、
「一問一答はできるのに、記述・計算になると解けない」ことです。
これは能力不足ではなく、
☆ 知識を“変換する練習”が足りていないだけ
というケースがほとんどです。
ここでは、
一問一答で覚えた知識を、どうやって記述問題・計算問題に変換するのか
を、入試で本当によく出る形に沿って解説します。
化学でよく出る記述・計算の聞かれ方
高校入試の化学では、次のような「聞かれ方」が非常に多いです。
① 理由を説明させる記述問題
例:
- なぜ反応の前後で質量が変わらないのか。
- なぜこの水溶液は酸性を示すのか。
☆ 単なる用語暗記ではなく、
「〜だから」という因果関係が求められます。
② 用語+計算を組み合わせた問題
例:
- 質量保存の法則を用いて、反応後の質量を求めなさい。
- 溶質・溶媒の関係を用いて、質量パーセント濃度を求めなさい。
☆ 一問一答で覚えた用語が“条件”として使われるのが特徴です。
③ 実験結果をもとに考えさせる問題
例:
- 実験装置の図を見て、起こっている変化を説明する。
- 実験前後の数値から、法則や性質を答える。
☆ 「この実験は何を確かめるものか?」
と考えられるかどうかがポイントです。
④ 空欄補充+理由説明のセット
例:
- ( )に当てはまる物質名を書き、そう考えた理由を説明しなさい。
☆ 一問一答レベルの知識+短文記述が必要になります。
短文記述・計算の考え方の型
ここからが最重要です。
化学の記述・計算は、毎回ゼロから考える必要はありません。
入試で使える「型」が決まっています。
記述問題の基本の型(化学)
結論 → 理由(〜だから)
例:
Q. 化学変化の前後で、全体の質量が変わらないのはなぜか。
A.
化学変化の前後で反応に関わった物質の種類は変わるが、
物質全体の量は変わらないから。
☆ このとき使っている知識は、
一問一答で覚えた「質量保存の法則」そのものです。
酸・アルカリ記述の型
性質 → 出すイオン → 結果
例:
Q. この水溶液がアルカリ性と判断できる理由を答えなさい。
A.
この水溶液は水酸化物イオンを出すため、アルカリ性である。
☆「アルカリ性=水酸化物イオンを出す」
という一問一答が、そのまま文章になります。
計算問題の考え方の型(質量%)
① 何を求めるか確認
② 溶質・溶媒・溶液を整理
③ 公式に当てはめる
例:
質量%濃度 = 溶質 ÷ 溶液 × 100
☆ 一問一答で
- 溶質とは何か
- 溶液とは何か
を理解していないと、式に入れる数字を間違えます。
実験問題の変換の型
実験の目的 → 操作 → 結果 → 分かること
例:
- 何を確かめる実験か
- どんな変化が起きたか
- そこから言える法則・性質は何か
☆ 実験問題は、
一問一答をストーリーとしてつなげる問題です。
メイン記事「記述変換テンプレ図」との併用が最強
ここまで解説した
- 記述の型
- 計算の考え方
は、図で整理すると一気に理解しやすくなります。
関連記事
☆ 「高校入試 理科 一問一答|記述変換テンプレ図」
では、
- 一問一答
→ 短文記述
→ 本番レベル記述
への変換をテンプレ図で可視化しています。
まとめ|一問一答は「ゴール」ではなく「スタート」
- 一問一答:知識を即答できるようにする
- 記述・計算:その知識を使って説明・処理する
この2段階を意識するだけで、
化学は一気に「得点源」に変わります。
入試直前チェック|化学で落としやすいポイント
高校入試直前期になると、「難問が解けない」よりも
「本当は取れるはずの問題を落とす」ことが合否を分けます。
ここでは、化学分野で特に失点が多い典型パターンを整理します。
イオン・反応式の暗記ミス
化学の失点原因で最も多いのが、
☆ 「分かっているつもり」の暗記ミスです。
よくあるミス① イオンの+−の取り違え
- 陽イオン(+)と陰イオン(−)を逆に書く
- 水素イオンと水酸化物イオンを混同する
これは知識不足ではなく、
確認不足によるケアレスミスです。
▶ 対策
- 一問一答で「イオン名+電気の種類」を必ずセットで確認
- 書く前に「+か−か」を一瞬声に出して確認
よくあるミス② 化学反応式の左右・原子数ミス
- 反応物と生成物を逆に書く
- 原子の数が左右でそろっていない
特に入試では、
反応式そのものが正しいかどうかを見られています。
▶ 対策
- 反応式は「意味」を理解して覚える
- 書き終わったら
「原子の数が左右で同じか」を必ずチェック
よくあるミス③ 用語は合っているが説明がズレている
例:
- 質量保存の法則の説明があいまい
- 中和の説明に「水」が抜けている
▶ 対策
- 一問一答の答えを一文で言い切れるかを確認
- 記述変換テンプレ(親記事)で最終チェック
計算問題の単位・条件見落とし
計算問題で落とす原因の多くは、
計算力不足ではなく「読み落とし」です。
よくあるミス① 単位を見ていない
- g と kg
- % を小数に直していない
▶ 対策
- 式を書く前に単位だけ先にチェック
- 濃度は「% → 小数」に直してから計算
よくあるミス② ふた付き・ふたなしの見落とし
- ふた付き容器なのに質量が変わると考えてしまう
- 気体が逃げる条件を考慮していない
▶ 対策
- 問題文の
「ふたをした」「密閉した」
という言葉に必ず線を引く - 質量保存が使えるかを最初に判断
よくあるミス③ 何を求めるか確認していない
- 溶質を求める問題なのに溶液を答える
- 水の質量を聞かれているのに食塩を書く
▶ 対策
- 計算前に
「最終的に答えるのは何か」を言葉で確認 - 答えの単位が合っているかを見る
入試直前チェックリスト(化学)
| チェック | 確認項目 | 最終確認ポイント |
|---|---|---|
| □ | イオン | 陽イオン・陰イオンの+−を間違えていないか |
| □ | イオン | 水素イオン/水酸化物イオンを混同していないか |
| □ | 反応式 | 反応物と生成物の左右を正しく書けるか |
| □ | 反応式 | 原子の数が左右でそろっているか |
| □ | 単位 | g・kg・%などの単位を見落としていないか |
| □ | 単位 | 答えの単位が問題文と一致しているか |
| □ | 条件 | 「ふたをする」「密閉する」などの条件を読んだか |
| □ | 条件 | 気体が逃げる/逃げないを正しく判断できているか |
| □ | 条件 | 何を求める問題か(溶質・溶媒・溶液)を確認したか |
| □ | 総合 | 見直しで計算・記述のミスを再チェックしたか |
本番直前は、新しい問題に手を出すより
このチェックリストを1問ごとに確認するだけで間違いを防げます。
化学分野のおすすめ問題集
入試直前期は、
問題集を増やすより「1冊を完璧にする」ことが最重要です。
ここでは、
☆ 一問一答で知識を固めたあとに使う問題集
として、基礎〜標準レベルで最適な選び方を解説します。
※以下の記事でさらにくわしく化学の対策問題集を紹介しています。
【高校入試】化学のおすすめ問題集9選|一問一答→記述・計算まで対応【2026年最新版】
基礎〜標準レベルは「1冊厳選」が正解
化学は、
- 出題パターンがある程度決まっている
- 同じ知識を使い回す問題が多い
という特徴があります。
そのため、
- 問題集を何冊も中途半端にやる
よりも - 1冊を3周以上やる
ほうが、確実に点につながります。
ほかの問題集も使いたい場合は、1冊を仕上げてからがおすすめです。
一問一答 → 問題集 の正しい使い分け
- 一問一答
→ 用語・法則を即答レベルにする - 問題集
→ その知識を「使う練習」をする
この役割分担を守ると、
化学は短期間で安定した得点源になります。
おすすめ問題集は別記事で詳しく解説
具体的な
- 書店で失敗しにくい問題集
- 偏差値帯別の向いている1冊
- 化学が苦手な人向け/得意な人向け
については、
☆ 別記事で詳しく解説しています。
→ 「高校入試 化学 おすすめ問題集」(作成中)
※本記事(化学一問一答)
→ 孫記事(化学問題集)
という流れで使うと、学習効率が最も高くなります。
まとめ|最後に点を落とさない人が合格する
- 化学は「難問」より「ミス」で落ちる
- イオン・反応式は直前チェック必須
- 計算は単位・条件・聞かれている内容を見る
この3点を意識するだけで、
入試本番の安定感が大きく変わります。
よくある質問Q&A(化学)
ここでは、高校入試化学で実際に相談が多い悩みをQ&A形式でまとめました。
一問一答学習と組み合わせて使うことで、弱点をその場で解消できます。
Q1. 化学の計算問題がどうしても苦手です。どう対策すればいいですか?
A. 計算力ではなく「整理力」が原因のことがほとんどです。
化学計算は、
- 溶質・溶媒・溶液
- 何を求めるか
を整理できれば、使う式はほぼ決まっています。
一問一答で用語を即答できる状態を作り、
→ その用語を使う計算問題を1パターンずつ練習する
のが最短ルートです。
Q2. 質量%濃度の問題で毎回混乱します。
A. 「何÷何か」を言葉で確認してください。
質量%濃度は必ず
☆ 溶質 ÷ 溶液 × 100
計算前に
「溶けている物質はどれ?」
「全体はどこまで?」
と日本語で確認するとミスが激減します。
Q3. イオンが覚えられません。+−がごちゃごちゃになります。
A. イオンは単独暗記をやめて「セット」で覚えましょう。
おすすめは、
- 名前+電気の種類(陽/陰)
- 出る場面(酸・アルカリ・電池)
を必ずセットで確認することです。
一問一答で
「水素イオン(+)」
「水酸化物イオン(−)」
のように声に出すと定着しやすくなります。
※なお、中3で習うイオンについて、以下の記事で実験種類別に詳しく解説しています。
【中3化学】塩酸の電気分解:塩酸に電気を流したときの化学反応の解説と練習問題
水酸化ナトリウムの電気分解:陽極陰極での反応や用語の解説(練習問題付き)
Q4. 電池の問題が苦手です。
A. 電池は暗記より「流れ」を理解すると楽になります。
電池は、
- 化学変化が起きる
- 電子が移動する
という1本のストーリーで整理すると解けます。
細かい反応よりも、
「どちらからどちらへ電子が動くか」
をまず押さえましょう。
Q5. 化学反応式が覚えられません。
A. 反応式は「意味」を理解して覚えるのが近道です。
丸暗記ではなく、
- 何と何が反応して
- 何ができるか
を言葉で説明できるようにすると、
反応式も自然に書けるようになります。
※なお、高校入試までに覚えておくべき化学反応式を以下の記事で詳しく解説しています。
覚えておくべき化学反応式の一覧(分解、酸化、還元、化合、沈殿、中和)
Q6. 反応式で原子数をそろえるのが苦手です。
A. 最後に「数チェック」する習慣をつけましょう。
反応式は、
書き終わったあとに
☆ 原子の数を左右で必ず確認
これだけで失点が激減します。
※なお、化学反応式のつくりかた(原子数のそろえかた)を以下の記事で詳しく解説しています。
化学反応式の作り方を完全解説!元素記号や分子の書き方、原子の数の合わせ方を解説
Q7. 記述問題になると何を書けばいいか分かりません。
A. 「結論→理由」の型を使ってください。
化学の記述はほぼすべて、
結論 → なぜなら〜だから
の形で書けます。
一問一答で覚えた用語を、
そのまま文章に変換する意識が大切です。
※詳しくはメイン記事の「記述変換テンプレ図」を参照してください。
Q8. 実験問題が難しく感じます。
A. 実験は「何を確かめたいか」を先に考えましょう。
実験問題は、
- 実験の目的
- 結果
- 分かること
をつなぐ問題です。
一問一答で覚えた法則・性質が、
どれを使う実験かを考えると整理しやすくなります。
Q9. 化学はどこから勉強するのが効率的ですか?
A. 化学変化 → 質量計算 → イオンの順がおすすめです。
この順番は、
- 出題率が高い
- 他分野につながる
という理由で、最も得点効率が良い流れです。
Q10. 一問一答だけで入試は対応できますか?
A. 一問一答は「スタート」で、ゴールではありません。
一問一答
→ 計算・記述
→ 問題集
この流れを作ることで、
一問一答が本番で使える知識に変わります。
Q11. 化学が苦手でも点は伸びますか?
A. 化学は最も「伸ばしやすい」分野です。
暗記と計算の型がはっきりしているため、
正しい順番で対策すれば、
短期間でも安定した得点源になります。
まとめ:化学は「覚える+使う」で安定得点が狙える
高校入試化学で重要なのは、
暗記か理解か、ではありません。
- 用語を覚える
- その用語を使って計算・記述する
この接続ができるかどうかが、得点差になります。
一問一答を軸にすると効率がよい理由
- 知識の抜け漏れを防げる
- 記述・計算の土台になる
- 短時間でも復習しやすい
だからこそ、
化学対策の中心に一問一答を置くのが最も効率的です。
他分野とあわせて理科全体を完成させよう
理科は、
- 物理
- 化学
- 生物
- 地学
をバランスよく得点することが重要です。
とあわせて学習すれば、
理科全体の得点力が一段階上がります。
まずはこの「化学一問一答」を何度も回し、
覚えた知識を“使える得点”に変えることから始めてください。
――――――――――
この記事を書いた人
現役の塾経営者。指導歴25年以上、のべ3,500人以上の小・中・高校生を指導。
定期テスト対策から中学・大学受験、英検対策まで幅広く対応。
→ 運営者情報はこちら
――――――――――


コメント