化学反応式を苦手にしている中学生・高校生は多いですよね。
暗記しようにも暗号のような元素記号が並び、さらに元素記号にはなかった数字(原子数)までついてきます。
ですが、化学反応式はつくり方を覚えれば勉強しやすくなり、テストでも高得点をねらえる範囲です。
そこで、化学反応式のつくり方を説明し、練習問題を用意しました。
※関連記事:化学反応式の一覧(分解、酸化、還元、化合、沈殿、中和
そもそも化学反応式とは?
化学反応式とは、化学反応を記号で表したものです。
化学反応では、ある物質(反応物)が別の物質(生成物)に変わります(酸素と水素が化合して水が発生する、など)。このとき、化学反応式を使って、どのような物質が反応し、何が生成されるかをわかりやすく示します。
化学反応式は、単に物質の変化を表すだけでなく、反応前後で物質の量や構成する原子の数が等しいことを示すため、質量保存の法則に基づいてバランスが取られています。
例えば、水素と酸素から水ができる場合、反応式は次のように書かれます。
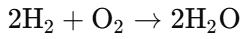
この式は、水素分子(H₂)が酸素分子(O₂)と反応して水(H₂O)が生成されることを表しています。
化学反応式のつくり方

化学反応式は3つのステップでつくれます。
物質名を元素記号で書く
まず、化学反応している物質名を元素記号にしましょう。
例えば水素を燃焼すると酸素と混ざって水になります。「水素」「酸素」を元素記号にしましょう。
水素→H
酸素→O
反応物(反応に使われる物質)と生成物(反応によってできる物質)を矢印「→」で区別します。左側に反応物、右側に生成物を書きます。
化学式にすると、以下のようになります。
H+O→H2O
分子の形に書きかえる
つづいて、先ほどの元素記号を分子に置きかえます。HはH2、OはO2です。
化学式にすると、以下のようになります。
H2+O2→H2O
原子の数を合わせる
最後に、左側の辺と右側の辺で原子の数を合わせます。
先ほどつくった「H2+O2→H2O」の式だと原子の数が以下のようになっています。
左側:Hが2つ、Oが2つ
右側:Hが2つ、Oが1つ
Hの原子数は合っていますが、Oの原子数が違っています。右側(H2O)にOを2つにする必要があります。
ただ、H2O2とすると水ではなく別の物質(過酸化水素水)になってしまうので、2H2Oとします。
すると、HとOの原子数は以下のようになります。
2×(H+H)=Hが4つ
2×O=Oが2つ
右側の式でHの数が4つになりました。左側のHは2つしかないので、4つにするためH2に2をかけて2H2とします。
これで左側も右側もHが4つ、Oが2つと同数になりました。
このようにして、化学反応式では左側の式と右側の式の「原子の数」を同じに調整してあげます。これを「質量保存の法則」と呼びます。
テストによく出る化学反応式の例
テストによく出る化学反応式を例題にして、化学反応式のつくり方を解説します。
硫酸銅(Ⅱ)と鉄の酸化還元反応の例題
硫酸銅(Ⅱ)(CuSO₄)と鉄(Fe)が反応して、鉄(Ⅱ)硫酸塩(FeSO₄)と銅(Cu)が生成される反応は、よくテストに出題される酸化還元反応の例です。
例題:
「硫酸銅(Ⅱ)に鉄(亜鉛版)を加えるとどうなりますか? 反応式を完成させなさい。」
解答と解説
反応式は次のようになります。
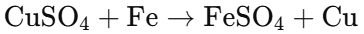
解説:
- 硫酸銅(Ⅱ)の化学式は CuSO₄
- 鉄の化学式は Fe
- 生成物は FeSO₄(鉄(Ⅱ)硫酸塩)と Cu(銅)
この反応では、銅イオン(Cu²⁺)が電子を受け取り、鉄(Fe)が電子を失うため、銅が還元され、鉄が酸化されます。
Cu、So4、Feそれぞれの原子数が左右で等しくなっているかを確認しておきましょう。
塩酸と水酸化ナトリウムの反応式の例題
中和反応は、酸と塩基が反応して水と塩ができる反応です。テストでよく出るのが、塩酸(HCl)と水酸化ナトリウム(NaOH)の反応です。
例題:
「酸と塩基を混ぜるとどうなりますか。化学反応式を書いてください。」
解答と解説
反応式は次の通りです。
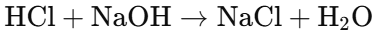
- HCl(塩酸)が酸、NaOH(水酸化ナトリウム)が塩基です。
- 生成物は塩化ナトリウム(NaCl)と水(H₂O)です。
重要ポイント:中和反応では、1モルの酸が1モルの塩基と反応することで、必ず水が生成されます。この比率を意識することで、原子数を調整しやすくなります。
テスト頻出の化学反応式一覧
テストによく出る化学反応式をいくつか載せておきます。
酸化銅と水素の反応:
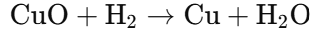
マグネシウムの燃焼(酸化):
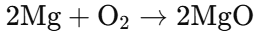
メタンの完全燃焼の化学反応式(二酸化炭素と水が生成):
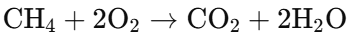
基礎レベルの化学式の練習問題
まずは、化学反応式の基礎的な問題から始めましょう。
練習問題
以下の化学反応式の空欄に入る数字を答えてください。
(1)水素+酸素→水
___H2+___O2→___H2O
(2)炭素+酸素→二酸化炭素
___C+___O2→___CO2
(3)マグネシウムの酸化(マグネシウム+酸素→酸化マグネシウム)
___Mg+___O2→___MgO
(4)塩素+ナトリウム→塩化ナトリウム
___Na+___Cl2→___NaCl
解答と解説
(1)2H2+O2→2H2O
解説:水素(H₂)が2つ、酸素(O₂)が2つ必要です。
(2)C+O2→CO2
解説:炭素(C)1つと酸素(O₂)1つです。
(3)2Mg+O2→2MgO2
解説:酸素(O₂)が2つ必要なので、マグネシウムも2つにします。
(4)2Na+Cl2→2NaCl2
解説:塩素(Cl₂)が2つあるため、ナトリウムも2つにします。
テストによく出る化学反応式の練習問題

それでは、テストによく出る化学反応式をつくる練習問題を解いてみましょう。
酸化銅の化学反応式
「銅」を加熱すると「酸素」と結びついて「酸化銅」になります。
この現象を化学反応式で表してください。
解答
2Cu+O2→2CuO
酸化マグネシウムの化学反応式
「マグネシウム」を加熱すると「酸素」と結びついて「酸化マグネシウム」になります。
この現象を化学反応式で表してください。
解答
2Mg+O2→2MgO
塩化銅の化学反応式
「銅」と「塩素」を結合させると「塩化銅」になります。
この現象を化学反応式で表してください。
解答
Cu+Cl2→CuCl2
硫化鉄の化学反応式
「鉄」と「硫黄」を結合させると「硫化鉄」になります。
この現象を化学反応式で表してください。
解答
Fe+S→FeS
硫化銅の化学反応式
「銅」と「硫黄」を結合させると「硫化銅」になります。
この現象を化学反応式で表してください。
解答
Cu+S→CuS
もっと練習したい人は教科書ワークが便利です。基本レベルから標準レベルまで、教科書に合わせた解説と演習問題が載っています。

中学教科書ワーク 理科 2年 東京書籍版 (オールカラー,付録付き)
中学生が覚えておくと役立つ化学反応式の一覧
| 化学反応式 | 化学反応の内容 |
| 2Ag2O→4Ag+02 | 酸化銀を熱すると銀と酸素に分かれる |
| 2H2O→2H2+O2 | 水を電気分解すると水素と酸素に分かれる |
| 2NaHCO3→Na2CO3+CO2+H2O | 炭酸水素ナトリウムを熱すると炭酸ナトリウムと二酸化炭素と水に分かれる |
| CuCl2→Cu+Cl2 | 塩化銅水溶液を電気分解すると銅と塩素に分かれる |
| 2HCl→H2+Cl2 | 塩酸を電気分解すると水素と酸素に分かれる |
| 2H2O2→2H2O+O2 | うすい過酸化水素水に二酸化マンガンを加えると、過酸化水素が水と酸素に分かれる |
| Fe+S→FeS | 鉄と硫黄を結合させると硫化鉄になる |
| Cu+S→CuS | 銅と硫黄を結合させると硫化銅になる |
| Cu+Cl2→CuCl2 | 銅と塩素を結合させると塩化銅になる |
| C+O2→CO2 | 炭素を燃焼させると二酸化炭素が発生する |
| S+O2→SO2 | 硫黄を燃焼させると二酸化硫黄になる |
| 3Fe+2O2→Fe3O4 | スチールウールを燃焼させると酸化鉄になる |
| 2Mg+O2→2MgO | マグネシウムと酸素を結合させると酸化マグネシウムになる |
| 2Cu+O2→2CuO | 銅を加熱すると酸化銅になる |
| 2H2+02→2H2O | 水素と酸素を結合させると水になる |
| 2CuO+C→2Cu+Co2 | 酸化銅と炭素の混合物を加熱すると銅と二酸化炭素になる |
| CuO+H2→Cu+H2O | 酸化銅と水素の混合物を加熱すると銅と水になる |
| 2Fe2O3+3C→4Fe+3CO2 | 酸化鉄と炭素の混合物を加熱すると鉄と二酸化炭素になる |
| Fe3O4+4H2→3Fe+4H2O | 酸化銅と炭素の混合物を加熱すると銅と水になる |
| CO2+2Mg→C+2MgO | 火をつけたマグネシウムを二酸化炭素のなかに入れると炭素と酸化マグネシウムになる |
なお、高校生が覚えておくべき化学反応式は以下の記事で紹介しています。
高校生が覚えておくべき化学反応式の一覧(分解、酸化、還元、化合、沈殿、中和)
化学反応式の原子の数をうまく合わせられないときの対処法
まずは単体から合わせる
化学反応式でバランスを取る際、単体の分子(H₂、O₂など)から数を合わせると簡単です。反応物と生成物に含まれる同じ元素を優先的に一致させると、全体で数を合わせやすくなります。
例えば、以下の化学反応式をご覧ください。
H2+O2→H2O
- 酸素(O)を見ると、右側(H₂O)の酸素原子が1つ不足しています。
- H₂Oに係数2をつけて調整します。
2H2+O2→2H2O
これで、Hが左も右も4つずつで、Oが2つずつで同数になりました。
覚えておきたい化学反応の基本パターン
化学反応式は、ひとつひとつ全くの別物というわけではありません。良く出る化学反応のパターンを覚えておくと、多くの化学反応式を覚えやすくなります。
例えば、以下の3パターンの化学反応を覚えておくのがおすすめです。
- 酸化反応:金属 + 酸素 → 酸化物
- 中和反応:酸 + 塩基 → 塩 + 水
- 燃焼反応:炭化水素 + 酸素 → 二酸化炭素 + 水
これらの基本パターンを押さえておくと、反応式がスムーズに作れます。
化学反応式を効率的に覚えるための勉強法
化学反応式を覚えるのには、いくつかおすすめの勉強法があります。
書いて覚える
化学反応式は、実際に手を動かして書くことで覚えやすくなります。まずは基本的な反応式を書き、次にバランスを取る練習を繰り返してください。
【おすすめの練習方法】
- 反応式を書き出す。
- バランスを取る。
- 答え合わせをする。
過去問を使って反復練習する
過去問には、頻出の化学反応式が多く含まれているため、テスト対策に最適です。定期テストや入試の過去問を解き、間違えた部分を何度も解きなおすことで、効率的に記憶が定着します。
【ポイント】
- 同じ反応式が出題されるパターンを確認する。
- 解いた問題は3回以上繰り返すと記憶が定着しやすくなります。
化学反応式に関する中学生・高校生向けQ&A
Q1: 化学反応式って何ですか?
A: 化学反応式は、物質がどのように変化するかを表す式です。反応に参加する物質(反応物)と、反応の結果できる物質(生成物)を元素記号や化学式で表し、反応の前後で原子の数が同じになるようにバランスを取るのが特徴です。
例:水素と酸素が反応して水ができる反応は、
2H2+O2→2H2O
と書きます。
Q2: 化学反応式で「原子の数を一致させる」ってどういう意味ですか?
A: 「原子の数を一致させる」とは、反応式の左側(反応物)と右側(生成物)で、同じ種類の原子を同じ数にすることです。
例えば、水素と酸素から水ができる場合、以下のような化学反応式を書きます。
H2+O2→H2O
「→」の左に水素原子(H)が2つ、酸素原子(O)が2つあります。「→」右では水素原子が2つで酸素が1つしかありません。
原子を数を左と右で一致させるために、係数を使います。
正しい式:
2H2+O2→2H2O
2H2は、「H2が2個(合計4個)ある」という意味です。左の式はHが4つ、Oが2つなので、右の式でもHが4つ、Oが2つになるようにします。
Q3: 酸化銅の化学反応式はどう書きますか?
A: 銅(Cu)と酸素(O)が結合して酸化銅(CuO)になる反応です。化学反応式は次のように書きます。
2Cu+O2→2CuO
Q4:原子の数を一致させるコツはありますか?
A: はい、以下のようにしましょう。
- 水素や酸素など、別々に数を一致させる
例えば、水の生成反応の場合、
H2+O2→H2O
最初に水素原子を調整して、次に酸素を調整しましょう。左の式でHが2つあり、右の式にもHが2つあります。次に酸素(O)を見ると、左の式には2つあるのに右の式には1つしかありません。そこで、「H2O」に係数2をつけます。するとOの数が一致しました。代わりに右の式ではHが4つになったので、左の「H2」にも係数2をつけます。これで水素も酸素も数が一致しました。 - 複雑な化合物は最後に調整
例:炭酸水素ナトリウムの分解
2NaHCO3→Na2CO3+CO2+H2O
このように、1つの物質に複数の原子が含まれる場合は、最後に調整しましょう。
Q5: テストでよく出る化学反応式を教えてください。
A: テストでよく出る化学反応式には、次のようなものがあります。
- 水の生成
2H2+O2→2H2O - 炭酸水素ナトリウムの分解
2NaHCO3→Na2CO3+CO2+H2O2 - マグネシウムの酸化
2Mg+O2→2MgO
ポイント:これらは基本的な反応なので、必ず覚えておきましょう!
Q6: 効率的に化学反応式を覚える方法は?
A: 効率的に覚えるための方法を紹介します。
- 書いて覚える
反応式をノートに何度も書いて覚えると、記憶に残りやすくなります。 - 過去問を解く
実際のテスト問題に慣れるために、過去問を繰り返し解くと、反応式を覚えるだけでなく、バランス調整の練習にもなります。
Q7: 化学反応式を間違えやすいポイントは?
A: 間違えやすいポイントをいくつか紹介します。
- 係数を間違える
反応式の前に付ける数字(係数)を間違えることがあります。原子の数を確認してから書きましょう。 - 反応の向きを間違える(「→」の左と右を逆に書いてしまう)
反応物と生成物の位置を間違えないように注意しましょう。
まとめ
中学生向けに化学反応式のつくり方を解説しました。
化学反応式は、物質名を元素記号で表し、分子に書きかえ、原子の数をそろえると完成です。
練習用に酸化銅、酸化マグネシウム、硫化銅、硫化鉄の化学反応式の練習問題も用意しました。
また、化学反応式は丸覚えするより、先に現象を理解しておくと覚えやすいです。
化学反応式を得意にして理科のテストで高得点をねらいましょう!



コメント