化学で習う化学反応式を苦手にしている人は多いのではないでしょうか。
アルファベットがたくさん並び、何かの暗号のように見えるかもしれません。
ですが、化学反応式はテストでもよう問われますし、「どのような内容なのか」も一緒に覚えると点を取りやすくなります。
そこで、中学生・高校生が覚えておくべき化学反応式を一覧で紹介します。
化学反応式の覚え方も説明しているので、ぜひ化学を得意科目にしましょう!
※関連記事:【高校生】定期テストで90点以上を取れる勉強方法
※関連記事:化学反応式の作り方
覚えておくべき化学反応式の一覧
化学反応式を一覧で紹介します。それぞれの化学反応の内容も載せているので、一緒に覚えておきましょう。
なお、中学生は「分解」「酸化」「還元」「化合」の化学反応式を覚えておけば十分です。
分解の化学反応式と特徴
分解とは1つの物質が2つ以上の物質に分かれることです。
以下の化学反応式を覚えておきましょう。
| 化学反応式 | 化学反応の内容 |
| 2Ag2O→4Ag+02 | 酸化銀を熱すると銀と酸素に分かれる |
| 2H2O→2H2+O2 | 水を電気分解すると水素と酸素に分かれる |
| 2NaHCO3→Na2CO3+CO2+H2O | 炭酸水素ナトリウムを熱すると炭酸ナトリウムと二酸化炭素と水に分かれる |
| CuCl2→Cu+Cl2 | 塩化銅水溶液を電気分解すると銅と塩素に分かれる |
| 2HCl→H2+Cl2 | 塩酸を電気分解すると水素と酸素に分かれる |
| 2H2O2→2H2O+O2 | うすい過酸化水素水に二酸化マンガンを加えると、過酸化水素が水と酸素に分かれる |

化合の化学反応式と特徴
化合とは、2つ以上の物質を混ぜて結合させ1つの物質にすることです。
以下の化学反応式を覚えておきましょう。
| 化学反応式 | 化学反応の内容 |
| Fe+S→FeS | 鉄と硫黄を結合させると硫化鉄になる |
| Cu+S→CuS | 銅と硫黄を結合させると硫化銅になる |
| Cu+Cl2→CuCl2 | 銅と塩素を結合させると塩化銅になる |
酸化の化学反応式と特徴
酸化とは、物質が酸素と結びつくことです。「酸化-」か「二酸化-」という名称になります。
以下の化学反応式を覚えておきましょう。
| 化学反応式 | 化学反応の内容 |
| C+O2→CO2 | 炭素を燃焼させると二酸化炭素が発生する |
| S+O2→SO2 | 硫黄を燃焼させると二酸化硫黄になる |
| 3Fe+2O2→Fe3O4 | スチールウールを燃焼させると酸化鉄になる |
| 2Mg+O2→2MgO | マグネシウムと酸素を結合させると酸化マグネシウムになる |
| 2Cu+O2→2CuO | 銅を加熱すると酸素と結びついて酸化銅になる |
| 2H2+02→2H2O | 水素と酸素を結合させると水になる |
還元の化学反応式と特徴
還元とは、酸化した物質が酸素をうばわれることです。
以下の化学反応式を覚えておきましょう。
| 化学反応式 | 化学反応の内容 |
| 2CuO+C→2Cu+Co2 | 酸化銅と炭素の混合物を加熱すると銅と二酸化炭素になる |
| CuO+H2→Cu+H2O | 酸化銅と水素の混合物を加熱すると銅と水になる |
| 2Fe2O3+3C→4Fe+3CO2 | 酸化鉄と炭素の混合物を加熱すると鉄と二酸化炭素になる |
| Fe3O4+4H2→3Fe+4H2O | 酸化銅と炭素の混合物を加熱すると銅と水になる |
| CO2+2Mg→C+2MgO | 火をつけたマグネシウムを二酸化炭素のなかに入れると炭素と酸化マグネシウムになる |
中学生も高校生もここまでの化学反応式はすべて覚えておきましょう。
沈殿の化学反応式と特徴
沈殿とは、水に溶けにくい物質の微粒子が重力にひかれて液の底に沈むことです。
以下の化学反応式を覚えておきましょう。
| 化学反応式 | 化学反応の内容 |
| Ca(OH)2+Co2→CaCo3+H2O | 石灰水に二酸化炭素を吹き込むと炭酸カルシウムと水がつくられ炭酸カルシウムが沈殿する |
| NaCl+AgNO3→AgCl+NaNO3 | 塩化ナトリウムに硝酸銀水溶液を混ぜると塩化銀と硝酸ナトリウムになり、塩化銀が沈殿する |
| BaCl2+CuSO4→BaSO4+CuCl2 | 硫酸銅を塩化バリウムに混ぜると硫酸バリウムと塩化銅がつくられ、硫酸バリウムが沈殿する |
中和の化学反応式と特徴
中和とは、酸性とアルカリ性の水溶液を混ぜるとどちらの性質も持たない物質(水と塩)になることです。
以下の化学反応式を覚えておきましょう。
| 化学反応式 | 化学反応の内容 |
| HCl+NaOH→NaCl+H2O | 塩酸と水酸化ナトリウムを混ぜると塩化ナトリウムと水になる |
| H2SO4+Ba(OH)2→BaSO4+2H2O | 硫酸と水酸化バリウムを混ぜると硫酸バリウムと水になる |
| CH3COOH+NaOH→CH3COONa+H2O | 酢酸と水酸化ナトリウムを混ぜると酢酸ナトリウムと水になる |
| CH3COOH+NH3→CH3COONH4 | 酢酸とアンモニアと混ぜると酢酸アンモニウムになる |
アンモニアの構造式↓
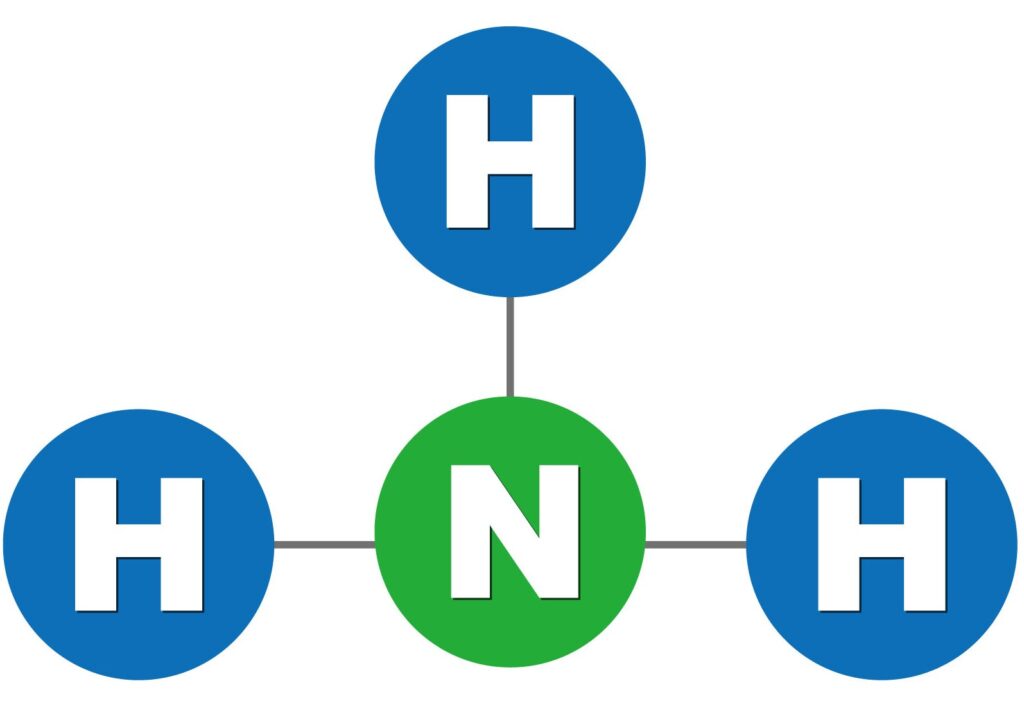
アンモニア分子のイメージ図↓
気体の発生の化学反応式と特徴
酸と金属や石灰石を混ぜて気体を発生させる化学反応式です。
| 化学反応式 | 化学反応の内容 |
| 2HCl+Mg→MgCl2+H2 | 塩酸とマグネシウムを混ぜると塩化マグネシウムと水素になる |
| HCl+NaHCO3→NaCl+CO2+H2O | 塩酸と炭酸水素ナトリウムを混ぜると塩化ナトリウムと二酸化炭素と水になる |
| 2HCl+CaCO3→CaCl2+CO2+H2O | 塩酸と炭酸カルシウムを混ぜると塩化カルシウムと二酸化炭素と水になる |
| FeS+2HCl→FeCl2+H2S | 硫化鉄と塩酸を混ぜると塩化鉄と硫化水素になる |
化学反応式の覚え方
化学反応式とは、さまざまな化学変化を、化学式を使って表したものです。
化学式をみれば「何が」「何に」変化したのかが分かるように書かれています。
なお、化学反応式のつくり方は以下の記事でくわしく解説しています。
【中学生・高校生向け】化学反応式の作り方を完全解説!元素記号や分子の書き方、原子の数の合わせ方を解説
化学反応の内容を覚える
化学反応式を覚えるにあたって、先に化学反応の内容を覚えましょう。
例えば「2H2+O2→2H2O」という化学反応式は「水素と酸素を化合して加熱すると、水になる」という内容を表しています。
「2H2+O2→2H2O」をいきなり丸暗記するのではなく、先に「どのような化学反応が起こっているのか」を覚えます。このほうが覚えやすく、忘れにくいからです。
物質量を合わせる
化学反応が起こる前と後(化学反応式の左側と右側)で物質量は変わりません。
例えば「2H2+O2→2H2O」では、左側の式にO2(酸素)とあります。Oが2つです。この数に合わせるためには、右側の式でH2O(水)のままだとOが1つ足りないため、2H2Oと2をつける必要があります(H2O2にすると過酸化水素水という別の物質になってしまうのでNG)。
2H2ですからHが4つ必要なので、左側の式でもH2に2を足して2H2とします。
このように、物質量を合わせるように式をいじると丸暗記に頼らなくても化学反応式を覚えやすくなります。
【頻出】高校化学のテストでよく出る化学反応TOP5
高校化学のテストでは、特定の化学反応がよく出題されます。以下は、過去問で頻出の重要反応をランキング形式で紹介します。
これらの反応をしっかり理解しておけば、テストで高得点を狙うことができます。
酸化還元反応:過マンガン酸カリウムの滴定反応
過マンガン酸カリウム(KMnO₄)を使った酸化還元滴定は化学の基本的な実験であり、頻繁にテストに登場します。
過マンガン酸カリウムは強力な酸化剤で、酸化還元反応を利用して他の物質を酸化することができます。
- 反応式例:過マンガン酸カリウムと過剰の塩酸を反応させ、酸化反応で還元されたMn²⁺が指示薬を使って色の変化を示します。
- テストで出やすいポイント:滴定時の色の変化の見極め方や、反応における酸化数の変化を理解することが重要です。
中和反応:酸と塩基の滴定
中和反応は、酸と塩基が反応して水と塩を生成する反応です。この反応は、酸の強さや塩基の強さ、滴定を通じて確認する実験方法としても登場します。
- 反応式例:HCl + NaOH → NaCl + H₂O
酸(HCl)と塩基(NaOH)が反応して水と塩(NaCl)を生成します。 - テストで出やすいポイント:中和滴定における指示薬の選び方や、酸・塩基の濃度を求める計算問題が出題されることが多いです。
付加反応:エチレンと臭素の反応
エチレン(C₂H₄)と臭素(Br₂)の反応は、アルケンの代表的な付加反応です。臭素がエチレンの二重結合に付加することで、新たな化合物が生成されます。
この反応は有機化学の基礎となるため、よく出題されます。
- 反応式例:C₂H₄ + Br₂ → C₂H₄Br₂
エチレンに臭素分子が付加して、1,2-ジブロモエタンが生成されます。 - テストで出やすいポイント:付加反応のメカニズムや、反応の速度に影響を与える条件を理解することが求められます。
沈殿反応:硝酸銀と塩化物イオンの反応
硝酸銀(AgNO₃)と塩化物イオン(Cl⁻)が反応すると、白色の塩化銀(AgCl)の沈殿が生成されます。沈殿反応は無機化学の中でも基本的な反応の一つです。
- 反応式例:AgNO₃ + NaCl → AgCl (沈殿) + NaNO₃
硝酸銀と塩化ナトリウムが反応して、塩化銀が沈殿として生成します。 - テストで出やすいポイント:沈殿の形成条件(温度や溶液の濃度など)や、沈殿反応を使ったイオンの識別問題がよく出題されます。
電気分解:水の電気分解
水の電気分解は、電気エネルギーを使って水を水素と酸素に分解する反応です。この反応は、電気化学の基本的な実験として広く利用されています。
- 反応式例:2H₂O → 2H₂ + O₂
水を電気分解すると、水素と酸素が発生します。 - テストで出やすいポイント:電解質の種類や電流の影響、陰極・陽極での反応の内容を理解することが重要です。
なお、水の電気分解と同様に塩酸の電気分解もよく出題されます。塩酸の電気分解については以下の記事でくわしく解説しています。
塩酸の電気分解:塩酸に電気を流したときの化学反応の解説と練習問題
化学反応を効率よく覚えるコツと勉強法
化学反応は覚える量が多く、単純に記憶するのは大変ですが、効率的に覚える方法があります。以下のコツを参考にして、しっかりと反応式を覚えましょう。
反応式のパターンを分類して覚える
化学反応にはいくつかのパターンがあります。酸化還元反応や中和反応、付加反応など、反応の種類ごとに特徴を捉えて分類して覚えると効率的です。
- 例:酸化還元反応は「酸化数の変化」、中和反応は「酸と塩基の反応」といったように、反応を分類してから覚えましょう。
反応を図で理解することで記憶を定着させる
化学反応式を文字で覚えるだけではなく、反応を視覚的に図で示すことで理解を深め、記憶を定着させることができます。反応のメカニズムや生成物を図にすると、より直感的に理解できます。
- 例:電気分解を図にして、陰極と陽極での反応を視覚的に表現して覚える方法です。
高校化学のおすすめ問題集
最後に、高校生向けに化学のテスト勉強に役立つ問題集を紹介します。
『高校これでわかる 化学』
1冊目は『高校これでわかる 化学』です。文英堂が出している基礎~標準レベルまでの参考書と問題集です。
参考書と問題集に分かれており単元名や並び順が同じなので、併用して勉強しやすいです。
学校の授業が分かりにくいとき、基礎からひとりで勉強しなおしたいときに便利です。
参考書↓

高校これでわかる 化学 (シグマベスト)
問題集↓

高校これでわかる基礎問題集 化学 (シグマベスト)
出版社:文英堂
『セミナー化学』
2冊目はセミナー化学です。『リードα』とよく併称される定番問題集です。
教科書レベルからMARCH、関関同立の入試レベルまで対応しており、解説も丁寧です。
問題数が非常に多いので、学校で配布された問題集のサブ教材として「もう少しくわしく知りたい」「もう少し問題演習をしたい」というときに使う人も多いです。

2023年度用 最新版 セミナー化学基礎+化学 問題集本体別冊解答編 新課程
出版社:第一学習社
まとめ
いかがでしょうか。
化学反応式を一覧で紹介し、化学反応式の覚え方を説明しました。分解、酸化、還元、化合、沈殿、中和、気体発生と化学反応の種類別にしています。
化学反応式は定期テストや入試によく出てきますが、丸暗記だけで点を取るのが難しい内容です。化学反応の内容を理解すると覚えやすく、テストで問題に答えやすくなります。
化学反応式をマスターして、化学を得意科目にしましょう!


コメント